11개월 만에 환자 투약 포함한 미국 임상 3상 재개 가능코오롱티슈진, 상폐위기 털고 기사회생할지 ‘주목’
코오롱티슈진은 미국 식품의약국(FDA)이 11일(이하 한국시간) 골관절염 세포유전자치료제 인보사 미국 임상 3상에 대한 보류를 해제, 3상 시험(환자투약)을 재개토록 했다고 12일 밝혔다.
FDA는 11일 코오롱티슈진에 보낸 ‘임상보류 해제’공문을 통해 “인보사에 대한 모든 임상보류 이슈들이 만족스럽게 해결됐다”며 “우리(FDA)는 임상보류를 해제했으며 코오롱티슈진은 인보사의 임상시험을 진행해도 좋다”고 전했다.
회사측은 FDA의 이번 결정이 회사가 이전까지 제출한 임상시험 데이터 유효성을 인정하며 이를 기초로 형질 전환된 신장유래세포(인보사2액)로 환자투약을 포함한 임상 3상 시험을 계속해도 좋다는 점을 인정해준 의미라고 설명했다.
FDA는 지난해 5월 3일 인보사 미국 임상 3상에 대해 임상보류를 결정하면서 인보사 구성 성분에 대한 특성 분석, 성분 변화 발생 경위, 향후 조치사항 등을 제출할 것을 요구했고 이어 9월 20일에는 1차 제출한 자료에 대한 보완자료를 추가로 요청했었다. 이에 따라 코오롱티슈진은 FDA 요청에 상응하는 실험 자료 등을 제출하며 협의해왔다.
FDA는 이번 문서에서 연례보고서에 제출된 인보사의 생산공정에 대한 개선 방안과 임상시료의 안정성에 대한 데이터를 추가로 요청했다. 코오롱티슈진 관계자는 “이번 요청은 이번 임상보류 해제와는 무관한 내용으로 충분히 해결할 수 있는 내용”이라고 말했다.
티슈진은 FDA와의 협의에 따라 임상시험계획서와 임상시험환자 동의서류 등에 대한 보완절차를 마치는대로 임상시험 환자투약을 진행할 예정이다. 코오롱티슈진 관계자는 “앞으로 진행할 미국 임상 3상 시험을 철저하게 수행해 세계 최초의 골관절염 세포유전자치료제로서의 인보사 가치를 입증하겠다”고 말했다.
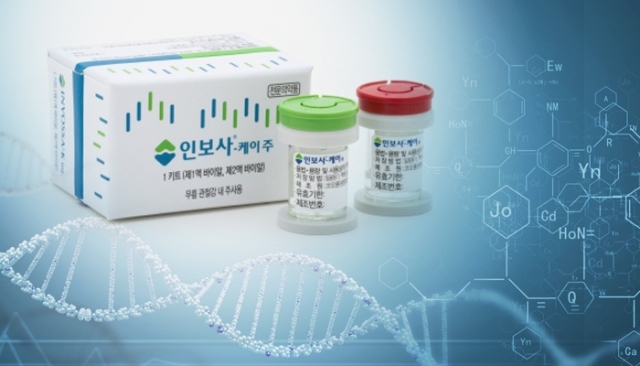
한편 인보사는 사람 연골에서 추출한 연골세포(제1액, HC)와 TGF-β1 유전자를 도입한 형질전환세포(제2액, TC)를 3:1의 비율로 섞어 관절강 내에 주사해 골관절염을 치료하는 세포유전자 치료제다.

뉴스웨이 이한울 기자
han22@newsway.co.kr
<저작권자 © 온라인 경제미디어 뉴스웨이 · 무단 전재 및 재배포 금지>





















댓글